பேட்டரிகள் எவ்வாறு வேலை செய்கின்றன மற்றும் வேலை செய்கின்றன
 தொழில்நுட்பத்தில் வார்த்தையின் பரந்த அர்த்தத்தில், "பேட்டரி" என்பது ஒரு குறிப்பிட்ட இயக்க நிலைமைகளின் கீழ் ஒரு குறிப்பிட்ட வகை ஆற்றலைக் குவிக்க அனுமதிக்கும் ஒரு சாதனத்தைக் குறிக்கிறது, மற்றவற்றில் அதை மனித தேவைகளுக்குப் பயன்படுத்துகிறது.
தொழில்நுட்பத்தில் வார்த்தையின் பரந்த அர்த்தத்தில், "பேட்டரி" என்பது ஒரு குறிப்பிட்ட இயக்க நிலைமைகளின் கீழ் ஒரு குறிப்பிட்ட வகை ஆற்றலைக் குவிக்க அனுமதிக்கும் ஒரு சாதனத்தைக் குறிக்கிறது, மற்றவற்றில் அதை மனித தேவைகளுக்குப் பயன்படுத்துகிறது.
ஒரு குறிப்பிட்ட காலத்திற்கு ஆற்றலைச் சேகரிக்க வேண்டிய இடத்தில் அவை பயன்படுத்தப்படுகின்றன, பின்னர் பெரிய உழைப்பு-தீவிர செயல்முறைகளை மேற்கொள்ள அதைப் பயன்படுத்துகின்றன. எடுத்துக்காட்டாக, பூட்டுகளில் பயன்படுத்தப்படும் ஹைட்ராலிக் குவிப்பான்கள் ஆற்றங்கரையில் கப்பல்கள் ஒரு புதிய நிலைக்கு உயர அனுமதிக்கின்றன.
மின்சார பேட்டரிகள் அதே கொள்கையில் மின்சாரத்துடன் வேலை செய்கின்றன: முதலில், அவை வெளிப்புற சார்ஜிங் மூலத்திலிருந்து மின்சாரத்தைக் குவிக்கின்றன (குவித்து) பின்னர் இணைக்கப்பட்ட நுகர்வோருக்கு வேலை செய்ய கொடுக்கின்றன. அவற்றின் இயல்பால், அவை இரசாயன மின்னோட்ட மூலங்களைச் சேர்ந்தவை, அவை அவ்வப்போது வெளியேற்றும் மற்றும் மீண்டும் மீண்டும் சார்ஜ் செய்யும் திறன் கொண்டவை.
செயல்பாட்டின் போது, எலக்ட்ரோட் தகடுகளின் கூறுகளுக்கு இடையில் அவற்றின் நிரப்புதல் பொருள் - எலக்ட்ரோலைட் மூலம் வேதியியல் எதிர்வினைகள் தொடர்ந்து நடைபெறுகின்றன.
மின் தொடர்புகளை வழங்குவதற்காக கம்பிகளுடன் வெவ்வேறு உலோகங்களின் இரண்டு தட்டுகள் கப்பலின் உடலில் செருகப்படும் போது, ஒரு பேட்டரி சாதனத்தின் திட்ட வரைபடத்தை எளிமைப்படுத்தப்பட்ட வரைதல் மூலம் குறிப்பிடலாம். தட்டுகளுக்கு இடையில் ஒரு எலக்ட்ரோலைட் ஊற்றப்படுகிறது.
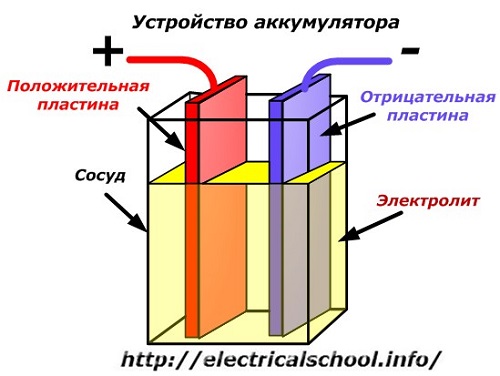
டிஸ்சார்ஜ் செய்யும்போது பேட்டரி செயல்பாடு
ஒரு ஒளி விளக்கைப் போன்ற ஒரு சுமை, மின்முனைகளுடன் இணைக்கப்படும் போது, ஒரு மூடிய மின்சுற்று உருவாக்கப்படுகிறது, இதன் மூலம் வெளியேற்ற மின்னோட்டம் பாய்கிறது. இது உலோக பாகங்களில் எலக்ட்ரான்கள் மற்றும் எலக்ட்ரோலைட்டில் உள்ள கேஷன்களுடன் அனான்களின் இயக்கத்தால் உருவாகிறது.
இந்த செயல்முறை வழக்கமாக நிக்கல்-காட்மியம் எலக்ட்ரோடு வடிவமைப்பு கொண்ட வரைபடத்தில் காட்டப்பட்டுள்ளது.
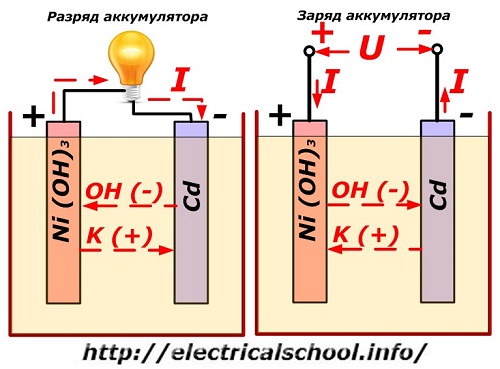
இங்கே, மின் கடத்துத்திறனை அதிகரிக்கும் கிராஃபைட் சேர்க்கைகள் கொண்ட நிக்கல் ஆக்சைடுகள் நேர்மறை மின்முனையின் பொருளாகப் பயன்படுத்தப்படுகின்றன. எதிர்மறை மின்முனையின் உலோகம் பஞ்சுபோன்ற காட்மியம் ஆகும்.
வெளியேற்றத்தின் போது, நிக்கல் ஆக்சைடுகளிலிருந்து செயல்படும் ஆக்ஸிஜன் துகள்கள் எலக்ட்ரோலைட்டில் வெளியிடப்பட்டு எதிர்மறை தட்டுகளுக்கு அனுப்பப்படுகின்றன, அங்கு காட்மியம் ஆக்ஸிஜனேற்றப்படுகிறது.
சார்ஜ் செய்யும் போது பேட்டரி செயல்திறன்
சுமை அணைக்கப்படும் போது, ஒரு நிலையான (சில சூழ்நிலைகளில், துடிக்கும்) மின்னழுத்தம் அதே துருவமுனைப்பு கொண்ட சார்ஜ் செய்யப்பட்ட பேட்டரியை விட அதிக மதிப்புள்ள தட்டு முனையங்களில் பயன்படுத்தப்படுகிறது, இது மூல மற்றும் நுகர்வோரின் பிளஸ் மற்றும் மைனஸ் டெர்மினல்கள் இணையும் போது .
சார்ஜர் எப்போதும் அதிக சக்தியைக் கொண்டுள்ளது, இது பேட்டரியில் எஞ்சியிருக்கும் ஆற்றலை "அடக்கி" வெளியேற்றத்தின் எதிர் திசையில் மின்னோட்டத்தை உருவாக்குகிறது. இதன் விளைவாக, மின்முனைகளுக்கும் எலக்ட்ரோலைட்டுக்கும் இடையே உள்ள உள் வேதியியல் செயல்முறைகள் மாறுகின்றன. உதாரணமாக, நிக்கல்-காட்மியம் தகடுகளின் பெட்டியில், நேர்மறை மின்முனை ஆக்ஸிஜனுடன் செறிவூட்டப்படுகிறது, மற்றும் எதிர்மறை - தூய காட்மியம் நிலைக்கு.
பேட்டரி டிஸ்சார்ஜ் செய்யப்பட்டு சார்ஜ் செய்யப்படும்போது, தட்டுகளின் (எலக்ட்ரோட்கள்) பொருளின் வேதியியல் கலவை மாறுகிறது, ஆனால் எலக்ட்ரோலைட் மாறாது.
பேட்டரி இணைப்பு முறைகள்
இணை இணைப்பு
ஒரு நபர் தாங்கக்கூடிய வெளியேற்ற மின்னோட்டத்தின் அளவு பல காரணிகளைப் பொறுத்தது, ஆனால் முதன்மையாக வடிவமைப்பு, பயன்படுத்தப்படும் பொருட்கள் மற்றும் அவற்றின் பரிமாணங்கள். மின்முனைகளில் உள்ள தட்டுகளின் பரப்பளவு பெரியது, அவை தாங்கக்கூடிய மின்னோட்டத்தை அதிகமாகக் கொண்டிருக்கும்.
மின்னோட்டத்தை சுமைக்கு அதிகரிக்க வேண்டியிருக்கும் போது, அதே வகை செல்களை இணையாக பேட்டரிகளில் இணைக்க இந்த கொள்கை பயன்படுத்தப்படுகிறது.ஆனால் அத்தகைய வடிவமைப்பை சார்ஜ் செய்ய, மூலத்தின் சக்தியை அதிகரிக்க வேண்டியது அவசியம். இந்த முறை ஆயத்த கட்டமைப்புகளுக்கு அரிதாகவே பயன்படுத்தப்படுகிறது, ஏனெனில் இப்போது தேவையான பேட்டரியை உடனடியாக வாங்குவது மிகவும் எளிதானது. ஆனால் அமில பேட்டரி உற்பத்தியாளர்கள் அதை பயன்படுத்துகின்றனர், வெவ்வேறு தட்டுகளை ஒற்றை தொகுதிகளாக இணைக்கின்றனர்.
தொடர் இணைப்பு
பயன்படுத்தப்படும் பொருட்களைப் பொறுத்து, 1.2 / 1.5 அல்லது 2.0 வோல்ட் மின்னழுத்தம் அன்றாட வாழ்க்கையில் பொதுவான இரண்டு மின்முனை தட்டுகளுக்கு இடையில் உருவாக்கப்படலாம். (உண்மையில், இந்த வரம்பு மிகவும் விரிவானது.) வெளிப்படையாக, இது பல மின் சாதனங்களுக்கு போதுமானதாக இல்லை. எனவே, அதே வகை பேட்டரிகள் தொடரில் இணைக்கப்பட்டுள்ளன, மேலும் இது பெரும்பாலும் ஒரு வழக்கில் செய்யப்படுகிறது.
அத்தகைய வடிவமைப்பின் ஒரு எடுத்துக்காட்டு கந்தக அமிலம் மற்றும் ஈய மின்முனை தகடுகளை அடிப்படையாகக் கொண்ட பரவலான வாகன வளர்ச்சி ஆகும்.
வழக்கமாக, மக்களிடையே, குறிப்பாக போக்குவரத்து ஓட்டுநர்களிடையே, எந்தவொரு சாதனத்தையும் பேட்டரி என்று அழைப்பது வழக்கம், அதன் கூறுகளின் எண்ணிக்கையைப் பொருட்படுத்தாமல் - பெட்டிகள். இருப்பினும், இது முற்றிலும் சரியானது அல்ல.தொடரில் இணைக்கப்பட்ட பல பெட்டிகளில் இருந்து கூடியிருந்த அமைப்பு, ஏற்கனவே ஒரு பேட்டரி ஆகும், இதற்கு சுருக்கமான பெயர் «АКБ» ஒட்டப்பட்டுள்ளது ... அதன் உள் அமைப்பு படத்தில் காட்டப்பட்டுள்ளது.
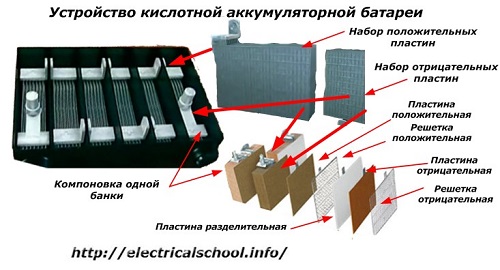
ஜாடிகளில் ஒவ்வொன்றும் நேர்மறை மற்றும் எதிர்மறை மின்முனைகளுக்கான தட்டுகளின் தொகுப்புடன் இரண்டு தொகுதிகள் உள்ளன. எலக்ட்ரோலைட் மூலம் நம்பகமான கால்வனிக் இணைப்பின் சாத்தியக்கூறுடன் உலோகத் தொடர்பு இல்லாமல் தொகுதிகள் ஒருவருக்கொருவர் பொருந்துகின்றன.
இந்த வழக்கில், தொடர்பு தட்டுகள் கூடுதல் கட்டம் மற்றும் ஒரு பிரிப்பான் தட்டு மூலம் ஒருவருக்கொருவர் பிரிக்கப்படுகின்றன.
தொகுதிகளில் தட்டுகளை இணைப்பது அவற்றின் வேலைப் பகுதியை அதிகரிக்கிறது, முழு கட்டமைப்பின் மொத்த எதிர்ப்பைக் குறைக்கிறது மற்றும் இணைக்கப்பட்ட சுமைகளின் சக்தியை அதிகரிக்க உங்களை அனுமதிக்கிறது.
பெட்டியின் வெளிப்புறத்தில், அத்தகைய பேட்டரி கீழே உள்ள படத்தில் காட்டப்பட்டுள்ள கூறுகளைக் கொண்டுள்ளது.
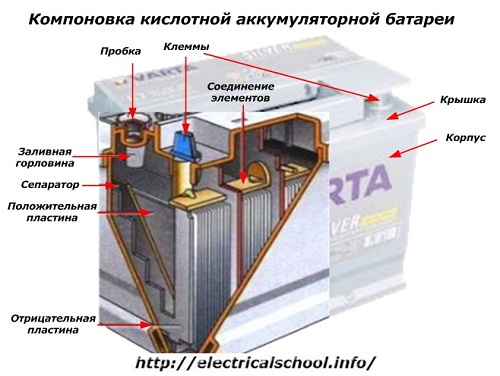
உறுதியான பிளாஸ்டிக் வீடுகள் ஒரு கவர் மூலம் சீல் செய்யப்பட்டு, காரின் மின்சுற்றுடன் இணைப்பதற்காக மேலே இரண்டு டெர்மினல்கள் (பொதுவாக கூம்பு வடிவ) பொருத்தப்பட்டிருப்பதைக் காட்டுகிறது. துருவமுனைப்பு அடையாளங்கள் அவற்றின் முனையங்களில் முத்திரையிடப்பட்டுள்ளன: «+» மற்றும் «- «. பொதுவாக நேர்மறை முனையம் வயரிங் பிழைகளைத் தடுக்க எதிர்மறை முனையத்தை விட சற்று பெரிய விட்டம் கொண்டது.
சர்வீஸ் செய்யக்கூடிய பேட்டரிகள் எலக்ட்ரோலைட் அளவைக் கட்டுப்படுத்த அல்லது செயல்பாட்டின் போது காய்ச்சி வடிகட்டிய தண்ணீரை சேர்க்க ஒவ்வொரு ஜாடியின் மேற்புறத்திலும் ஒரு நிரப்பு துளை உள்ளது. ஒரு பிளக் அதில் திருகப்படுகிறது, இது வழக்கின் உள் துவாரங்களை மாசுபாட்டிலிருந்து பாதுகாக்கிறது மற்றும் அதே நேரத்தில் பேட்டரி சாய்ந்திருக்கும் போது எலக்ட்ரோலைட் சிந்துவதைத் தடுக்கிறது.
சக்திவாய்ந்த கட்டணத்துடன், எலக்ட்ரோலைட்டிலிருந்து வாயுவை வெளியேற்றுவது சாத்தியமாகும் (மேலும் இந்த செயல்முறை தீவிர ஓட்டத்தின் போது சாத்தியமாகும்), பெட்டியின் உள்ளே அழுத்தம் அதிகரிப்பதைத் தடுக்க செருகிகளில் துளைகள் செய்யப்படுகின்றன.ஆக்ஸிஜன் மற்றும் ஹைட்ரஜன், அதே போல் எலக்ட்ரோலைட் நீராவிகள் அவற்றின் வழியாக வெளியேறுகின்றன. அதிகப்படியான சார்ஜிங் மின்னோட்டங்களை உள்ளடக்கிய இத்தகைய சூழ்நிலைகளைத் தவிர்க்க பரிந்துரைக்கப்படுகிறது.
அதே எண்ணிக்கை வங்கிகளுக்கு இடையில் உள்ள உறுப்புகளின் இணைப்பு மற்றும் எலக்ட்ரோடு தட்டுகளின் ஏற்பாடு ஆகியவற்றைக் காட்டுகிறது.
கார் ஸ்டார்டர் பேட்டரிகள் (லெட் ஆசிட்) இரட்டை சல்பேஷன் கொள்கையில் வேலை செய்கின்றன. வெளியேற்றம் / சார்ஜ் செய்யும் போது, அவற்றில் ஒரு மின் வேதியியல் செயல்முறை நடைபெறுகிறது, எலக்ட்ரோலைட்டில் (சல்பூரிக் அமிலம்) நீரின் வெளியீடு / உறிஞ்சுதலுடன் மின்முனைகளின் செயலில் உள்ள வெகுஜனத்தின் வேதியியல் கலவையில் மாற்றம் ஏற்படுகிறது.
சார்ஜ் செய்யும் போது எலக்ட்ரோலைட்டின் குறிப்பிட்ட ஈர்ப்பு அதிகரிப்பு மற்றும் பேட்டரி டிஸ்சார்ஜ் செய்யப்படும்போது குறைவதை இது விளக்குகிறது. வேறு வார்த்தைகளில் கூறுவதானால், பேட்டரியின் மின் நிலையை மதிப்பிடுவதற்கு அடர்த்தி மதிப்பு உங்களை அனுமதிக்கிறது. அதை அளவிட ஒரு சிறப்பு சாதனம் பயன்படுத்தப்படுகிறது - ஒரு கார் ஹைட்ரோமீட்டர்.
அமில பேட்டரிகளின் எலக்ட்ரோலைட்டின் ஒரு பகுதியாக இருக்கும் காய்ச்சி வடிகட்டிய நீர், ஒரு திட நிலையாக மாறும் - எதிர்மறை வெப்பநிலையில் பனி. எனவே, குளிர்ந்த காலநிலையில் கார் பேட்டரிகள் உறைவதைத் தடுக்க, விதிகளில் வழங்கப்பட்ட சிறப்பு நடவடிக்கைகளைப் பயன்படுத்துவது அவசியம். சுரண்டலுக்காக.
என்ன வகையான பேட்டரிகள் உள்ளன?
பல்வேறு நோக்கங்களுக்காக நவீன உற்பத்தியானது எலக்ட்ரோட்கள் மற்றும் எலக்ட்ரோலைட்டின் வெவ்வேறு கலவையுடன் மூன்று டஜன் தயாரிப்புகளை உற்பத்தி செய்கிறது. அறியப்பட்ட 12 மாதிரிகள் லித்தியத்தில் மட்டுமே இயங்குகின்றன.

பின்வருபவை எலக்ட்ரோடு உலோகமாகக் காணலாம்:
-
வழி நடத்து;
-
இரும்பு;
-
லித்தியம்;
-
டைட்டானியம்;
-
கோபால்ட்;
-
காட்மியம்;
-
நிக்கல்;
-
துத்தநாகம்;
-
வெள்ளி;
-
வெனடியம்;
-
அலுமினியம்
-
வேறு சில பொருட்கள்.
அவை மின் வெளியீட்டு பண்புகளை பாதிக்கின்றன, எனவே பயன்பாடு.
மின்சார ஸ்டார்டர் மோட்டார்கள் மூலம் உள் எரிப்பு இயந்திரங்களின் கிரான்ஸ்காஃப்ட்களின் சுழற்சியின் விளைவாக குறுகிய கால உயர் சுமைகளைத் தாங்கும் திறன் ஈய-அமில பேட்டரிகளின் சிறப்பியல்பு. அவை போக்குவரத்து, தடையில்லா மின்சாரம் மற்றும் அவசர சக்தி அமைப்புகளில் பரவலாகப் பயன்படுத்தப்படுகின்றன.
தரநிலை கால்வனிக் செல்கள் (வழக்கமான பேட்டரிகள்) பொதுவாக நிக்கல்-காட்மியம், நிக்கல்-துத்தநாகம் மற்றும் நிக்கல்-மெட்டல் ஹைட்ரைடு பேட்டரிகளால் மாற்றப்படுகின்றன.
ஆனால் லித்தியம்-அயன் அல்லது லித்தியம்-பாலிமர் வடிவமைப்புகள் மொபைல் மற்றும் கணினி சாதனங்கள், கட்டுமான கருவிகள் மற்றும் மின்சார வாகனங்களில் கூட நம்பகத்தன்மையுடன் செயல்படுகின்றன.
பயன்படுத்தப்படும் எலக்ட்ரோலைட் வகையின் படி, பேட்டரிகள்:
-
புளிப்பான
-
காரமானது.
நோக்கத்திற்கு ஏற்ப பேட்டரிகளின் வகைப்பாடு உள்ளது. எடுத்துக்காட்டாக, நவீன நிலைமைகளில், ஆற்றல் பரிமாற்றத்திற்குப் பயன்படுத்தப்படும் சாதனங்கள் தோன்றியுள்ளன - பிற ஆதாரங்களை ரீசார்ஜ் செய்தல். வெளிப்புற பேட்டரி என்று அழைக்கப்படுவது பல மொபைல் சாதனங்களின் உரிமையாளர்களுக்கு மாற்று மின் நெட்வொர்க் இல்லாத நிலையில் உதவுகிறது. இது டேப்லெட், ஸ்மார்ட்போன், மொபைல் போன் ஆகியவற்றை மீண்டும் மீண்டும் சார்ஜ் செய்யக்கூடியது.
இந்த பேட்டரிகள் அனைத்தும் ஒரே செயல்பாட்டுக் கொள்கை மற்றும் ஒத்த சாதனத்தைக் கொண்டுள்ளன. எடுத்துக்காட்டாக, கீழே உள்ள படத்தில் காட்டப்பட்டுள்ள லித்தியம்-அயன் விரல் மாதிரி பல வழிகளில் முன்பு விவாதிக்கப்பட்ட அமில பேட்டரிகளின் வடிவமைப்பை மீண்டும் செய்கிறது.
இங்கே நாம் அதே தொடர்பு மின்முனைகள், தட்டுகள், பிரிப்பான் மற்றும் வீடுகளைப் பார்க்கிறோம். மற்ற வேலை நிலைமைகளை கணக்கில் எடுத்துக்கொண்டு மட்டுமே அவை செய்யப்படுகின்றன.
பேட்டரியின் அடிப்படை மின் பண்புகள்
சாதனத்தின் செயல்பாடு அளவுருக்களால் பாதிக்கப்படுகிறது:
-
திறன்;
-
ஆற்றல் அடர்த்தி;
-
சுய வெளியேற்றம்;
-
வெப்பநிலை ஆட்சி.
திறன் பேட்டரியின் அதிகபட்ச சார்ஜ் என்று அழைக்கப்படுகிறது, இது வெளியேற்றத்தின் போது குறைந்த மின்னழுத்தத்திற்கு கொடுக்க முடியும். இது பதக்கங்கள் (SI அமைப்பு) மற்றும் ஆம்பியர்-மணிகளில் (அமைப்பு அல்லாத அலகு) வெளிப்படுத்தப்படுகிறது.
ஒரு வகை திறன் என, "ஆற்றல் திறன்" உள்ளது, இது குறைந்தபட்ச அனுமதிக்கப்பட்ட மின்னழுத்தத்திற்கு வெளியேற்றத்தின் போது வெளியிடப்பட்ட ஆற்றலை தீர்மானிக்கிறது. இது ஜூல்ஸ் (SI) மற்றும் வாட்-மணிகளில் (SI அல்லாத அலகுகள்) அளவிடப்படுகிறது.
ஆற்றல் அடர்த்தியானது மின்கலத்தின் எடை அல்லது அளவிற்கான ஆற்றலின் அளவின் விகிதமாக வெளிப்படுத்தப்படுகிறது.
டெர்மினல்களில் சுமை இல்லாத நிலையில் சார்ஜ் செய்த பிறகு திறன் இழப்பை சுய-வெளியேற்றம் கருதுகிறது. இது வடிவமைப்பைப் பொறுத்தது மற்றும் பல காரணங்களுக்காக மின்முனைகளுக்கு இடையில் உள்ள காப்பு முறிவுகளால் அதிகரிக்கிறது.
இயக்க வெப்பநிலை மின் பண்புகளை பாதிக்கிறது மற்றும் உற்பத்தியாளரால் குறிப்பிடப்பட்ட விதிமுறையிலிருந்து தீவிரமான விலகல்கள் ஏற்பட்டால், அது பேட்டரியை சேதப்படுத்தும். வெப்பமும் குளிர்ச்சியும் ஏற்றுக்கொள்ள முடியாதவை, அவை இரசாயன எதிர்வினைகளின் போக்கையும், பெட்டியின் உள்ளே சுற்றுச்சூழலின் அழுத்தத்தையும் பாதிக்கின்றன.
