எலக்ட்ரோலைட் என்றால் என்ன
அயனிகளின் இயக்கம் காரணமாக மின்சாரம் ஏற்படும் பொருட்கள், அதாவது. அயனி கடத்துத்திறன்எலக்ட்ரோலைட்டுகள் என்று அழைக்கப்படுகின்றன. எலக்ட்ரோலைட்டுகள் இரண்டாவது வகை கடத்திகளுக்கு சொந்தமானது, ஏனெனில் அவற்றில் உள்ள மின்னோட்டம் இரசாயன செயல்முறைகளுடன் தொடர்புடையது, மேலும் உலோகங்களைப் போல எலக்ட்ரான்களின் இயக்கத்துடன் அல்ல.
கரைசலில் உள்ள இந்த பொருட்களின் மூலக்கூறுகள் மின்னாற்பகுப்பு விலகல் திறன் கொண்டவை, அதாவது, நேர்மறையாக சார்ஜ் செய்யப்பட்ட (கேஷன்கள்) மற்றும் எதிர்மறையாக சார்ஜ் செய்யப்பட்ட (அயனிகள்) அயனிகளாக கரைக்கப்படும் போது அவை சிதைகின்றன. திட எலக்ட்ரோலைட்டுகள், அயனி உருகும் மற்றும் எலக்ட்ரோலைட் கரைசல்கள் இயற்கையில் காணப்படுகின்றன. கரைப்பான் வகையைப் பொறுத்து, எலக்ட்ரோலைட்டுகள் அக்வஸ் மற்றும் அல்லாத நீர், அத்துடன் ஒரு சிறப்பு வகை - பாலிஎலக்ட்ரோலைட்டுகள்.
நீரில் கரையும் போது பொருள் சிதைவடையும் அயனிகளின் வகையைப் பொறுத்து, H + மற்றும் OH- அயனிகள் இல்லாத எலக்ட்ரோலைட்டுகள் (உப்பு எலக்ட்ரோலைட்டுகள்), ஏராளமான H + அயனிகள் (அமிலங்கள்) மற்றும் OH- அயனிகளின் ஆதிக்கம் கொண்ட எலக்ட்ரோலைட்டுகள் ( அடிப்படை) தனிமைப்படுத்தப்படலாம்.
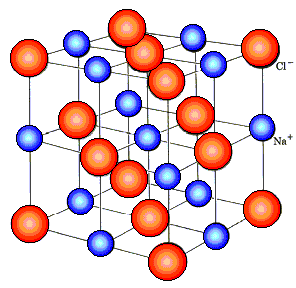
எலக்ட்ரோலைட் மூலக்கூறுகளின் விலகலின் போது சம எண்ணிக்கையிலான நேர்மறை மற்றும் எதிர்மறை அயனிகள் உருவாக்கப்பட்டால், அத்தகைய எலக்ட்ரோலைட் சமச்சீர் என்று அழைக்கப்படுகிறது.அல்லது கரைசலில் நேர்மறை மற்றும் எதிர்மறை அயனிகளின் எண்ணிக்கை ஒரே மாதிரியாக இல்லாவிட்டால் சமச்சீரற்றது. சமச்சீர் எலக்ட்ரோலைட்டுகளின் எடுத்துக்காட்டுகள் - KCl - 1,1-வேலண்ட் எலக்ட்ரோலைட் மற்றும் CaSO4 - 2,2-வேலண்ட் எலக்ட்ரோலைட். சமச்சீரற்ற எலக்ட்ரோலைட்டின் பிரதிநிதி, எடுத்துக்காட்டாக, H2TAKA4 - ஒரு 1,2-வேலண்ட் எலக்ட்ரோலைட்.

அனைத்து எலெக்ட்ரோலைட்டுகளையும் தோராயமாக வலுவான மற்றும் பலவீனமாக பிரிக்கலாம், அவை பிரிக்கும் திறனைப் பொறுத்து. நீர்த்த கரைசல்களில் உள்ள வலுவான எலக்ட்ரோலைட்டுகள் கிட்டத்தட்ட முழுமையாக அயனிகளாக சிதைகின்றன. இவற்றில் அதிக எண்ணிக்கையிலான கனிம உப்புகள், சில அமிலங்கள் மற்றும் நீர் கரைசல்களில் உள்ள தளங்கள் அல்லது ஆல்கஹால்கள், கீட்டோன்கள் அல்லது அமைடுகள் போன்ற அதிக விலகல் சக்தி கொண்ட கரைப்பான்கள் அடங்கும்.
பலவீனமான எலக்ட்ரோலைட்டுகள் பகுதியளவு மட்டுமே சிதைந்து, பிரிக்கப்படாத மூலக்கூறுகளுடன் மாறும் சமநிலையில் இருக்கும். இவற்றில் ஏராளமான கரிம அமிலங்களும் கரைப்பான்களில் உள்ள பல தளங்களும் அடங்கும்.
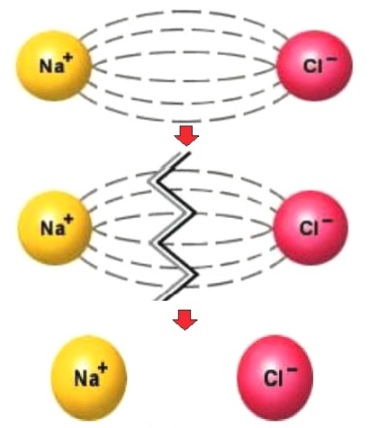
விலகலின் அளவு பல காரணிகளைப் பொறுத்தது: வெப்பநிலை, செறிவு மற்றும் கரைப்பான் வகை. எனவே, ஒரே எலக்ட்ரோலைட் வெவ்வேறு வெப்பநிலையில், அல்லது அதே வெப்பநிலையில் ஆனால் வெவ்வேறு கரைப்பான்களில், வெவ்வேறு டிகிரிகளில் பிரிக்கப்படும்.
மின்னாற்பகுப்பு விலகல், வரையறையின்படி, கரைசலில் அதிக எண்ணிக்கையிலான துகள்களை உருவாக்குவதால், இது எலக்ட்ரோலைட்டுகள் மற்றும் பல்வேறு வகையான பொருட்களின் இயற்பியல் பண்புகளில் குறிப்பிடத்தக்க வேறுபாடுகளுக்கு வழிவகுக்கிறது: ஆஸ்மோடிக் அழுத்தம் அதிகரிக்கிறது, கரைப்பான் தூய்மை தொடர்பாக உறைபனி வெப்பநிலை மாறுகிறது. மற்றும் பலர்.
எலக்ட்ரோலைட் அயனிகள் பெரும்பாலும் மின் வேதியியல் செயல்முறைகள் மற்றும் இரசாயன எதிர்வினைகளில் சுயாதீன இயக்க அலகுகளாக பங்கேற்கின்றன, கரைசலில் உள்ள மற்ற அயனிகளிலிருந்து சுயாதீனமாக உள்ளன: எலக்ட்ரோலைட்டில் மூழ்கியிருக்கும் மின்முனைகளில், எலக்ட்ரோலைட் வழியாக மின்னோட்டம் செல்லும் போது, ஆக்சிஜனேற்ற-குறைப்பு எதிர்வினைகள் நடைபெறுகின்றன. அவை எலக்ட்ரோலைட் கலவையில் சேர்க்கப்படுகின்றன.
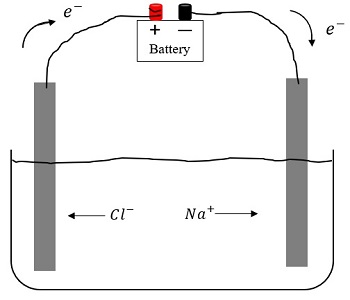
எனவே, எலக்ட்ரோலைட்டுகள் என்பது அயனிகள், கரைப்பான் மூலக்கூறுகள், பிரிக்கப்படாத கரைப்பான் மூலக்கூறுகள், அயனி ஜோடிகள் மற்றும் பெரிய சேர்மங்களை உள்ளடக்கிய பொருட்களின் சிக்கலான அமைப்புகளாகும். எனவே, எலக்ட்ரோலைட்டுகளின் பண்புகள் பல காரணிகளால் தீர்மானிக்கப்படுகின்றன: அயன்-மூலக்கூறு மற்றும் அயனி-அயன் தொடர்புகளின் தன்மை, கரைந்த துகள்களின் முன்னிலையில் கரைப்பானின் கட்டமைப்பில் மாற்றங்கள் போன்றவை.
துருவ எலக்ட்ரோலைட்டுகளின் அயனிகள் மற்றும் மூலக்கூறுகள் ஒருவருக்கொருவர் மிகவும் சுறுசுறுப்பாக தொடர்பு கொள்கின்றன, இது தீர்வு கட்டமைப்புகளை உருவாக்குவதற்கு வழிவகுக்கிறது, அயனிகளின் அளவு குறைதல் மற்றும் அவற்றின் மதிப்புகள் அதிகரிப்பதன் மூலம் இதன் பங்கு மிகவும் குறிப்பிடத்தக்கதாகிறது. தீர்வு ஆற்றல் என்பது கரைப்பான் மூலக்கூறுகளுடன் எலக்ட்ரோலைட் அயனிகளின் தொடர்புகளின் அளவீடு ஆகும்.
எலக்ட்ரோலைட்டுகள், அவற்றின் செறிவைப் பொறுத்து, அவை: நீர்த்த தீர்வுகள், நிலையற்ற மற்றும் செறிவூட்டப்பட்டவை. நீர்த்த கரைசல்கள் தூய கரைப்பான் கட்டமைப்பில் ஒத்திருக்கும், ஆனால் தற்போதுள்ள அயனிகள் அவற்றின் செல்வாக்கால் இந்த கட்டமைப்பை சீர்குலைக்கின்றன. வலுவான எலக்ட்ரோலைட்டுகளின் இத்தகைய பலவீனமான தீர்வுகள் அயனிகளுக்கு இடையிலான மின்னியல் தொடர்பு காரணமாக பண்புகளில் சிறந்த தீர்வுகளிலிருந்து வேறுபடுகின்றன.
அயனிகளின் செல்வாக்கின் காரணமாக கரைப்பான் கட்டமைப்பில் குறிப்பிடத்தக்க மாற்றத்தால் செறிவின் மாற்றம் பகுதி வகைப்படுத்தப்படுகிறது.இன்னும் அதிக செறிவில், பெரும்பாலான கரைப்பான் மூலக்கூறுகள் அயனிகளுடன் தீர்வு கட்டமைப்புகளில் பங்கேற்கின்றன, இதனால் கரைப்பான் பற்றாக்குறையை உருவாக்குகிறது.
செறிவூட்டப்பட்ட கரைசல் ஒரு அயனி உருகும் அல்லது படிக கரைப்புக்கு நெருக்கமான ஒரு அமைப்பைக் கொண்டுள்ளது, இது உயர் வரிசை மற்றும் அயனி கட்டமைப்புகளின் சீரான தன்மையால் வகைப்படுத்தப்படுகிறது. இந்த அயனி கட்டமைப்புகள் சிக்கலான இடைவினைகள் மூலம் ஒருவருக்கொருவர் மற்றும் நீர் மூலக்கூறுகளுடன் பிணைக்கப்படுகின்றன.
அவற்றின் பண்புகளின் உயர்-வெப்பநிலை மற்றும் குறைந்த-வெப்பநிலை பகுதிகள், அதே போல் உயர் மற்றும் சாதாரண-அழுத்த பகுதிகள், எலக்ட்ரோலைட்டுகளின் சிறப்பியல்பு. அழுத்தம் அல்லது வெப்பநிலை அதிகரிக்கும் போது, கரைப்பானின் மோலார் ஒழுங்குமுறை குறைகிறது மற்றும் கரைசலின் பண்புகளில் துணை மற்றும் தீர்வு விளைவுகளின் செல்வாக்கு பலவீனமடைகிறது. மேலும் வெப்பநிலை உருகும் இடத்திற்குக் கீழே குறையும் போது, சில எலக்ட்ரோலைட்டுகள் கண்ணாடி நிலைக்குச் செல்கின்றன. அத்தகைய எலக்ட்ரோலைட்டின் உதாரணம் LiCl இன் நீர்வாழ் கரைசல் ஆகும்.
இன்று, எலக்ட்ரோலைட்டுகள் தொழில்நுட்பம் மற்றும் உயிரியல் உலகில் குறிப்பாக முக்கிய பங்கு வகிக்கின்றன. உயிரியல் செயல்முறைகளில், எலக்ட்ரோலைட்டுகள் கனிம மற்றும் கரிம தொகுப்புக்கான ஒரு ஊடகமாகவும், தொழில்நுட்பத்தில் மின்வேதியியல் உற்பத்திக்கான அடிப்படையாகவும் செயல்படுகின்றன.
மின்னாற்பகுப்பு, மின்னாற்பகுப்பு, உலோகங்களின் அரிப்பு, மின் படிகமாக்கல் - இந்த நிகழ்வுகள் பல நவீன தொழில்களில், குறிப்பாக ஆற்றல் மற்றும் சுற்றுச்சூழல் பாதுகாப்பின் அடிப்படையில் முக்கியமான இடங்களை ஆக்கிரமித்துள்ளன.
மேலும் பார்க்க: நீரின் மின்னாற்பகுப்பு மூலம் ஹைட்ரஜன் உற்பத்தி - தொழில்நுட்பம் மற்றும் உபகரணங்கள்



