உலோகக்கலவைகளின் எதிர்ப்பு
பல உலோகங்கள் மற்றும் பல உலோகக் கலவைகள் உள்ளன.
மனித உலோகவியல் சோதனைகளிலிருந்து ஆரம்பகால செயற்கை கலவைகள் (தொல்பொருள் எச்சங்களின் அடிப்படையில்) கிமு 3000 முதல் 2500 வரை உருவாக்கப்பட்டன.
இது முதன்மையாக வெண்கலமாகும், ஏனெனில் இது இயற்றப்பட்ட உலோகங்கள் (தாமிரம் மற்றும் தகரம்) அவற்றின் சொந்த மாநிலத்தில் (ஏராளமாக) உள்ளன மற்றும் தாதுவிலிருந்து பிரித்தெடுக்க தேவையில்லை.
தங்கம் மற்றும் வெள்ளி ஆகியவை இயற்கையில் ஏராளமாக உள்ள உலோகங்கள் மற்றும் இந்த காரணத்திற்காக அவை கிமு 5 மில்லினியத்தில் இருந்து அறியப்படுகின்றன, எனவே அவை பெரும்பாலும் கலக்கப்படுகின்றன, குறிப்பாக தங்கத்தின் நிறம் அல்லது கடினத்தன்மையை மாற்ற .
கோட்பாட்டில், எண்ணற்ற உலோகக் கலவைகள் உள்ளன. அடிப்படை செயல்முறை எளிதானது: இரண்டு அல்லது அதற்கு மேற்பட்ட உலோகங்களை அவை பொருத்தமான உருகுநிலையை அடையும் வரை சூடாக்கவும், பின்னர் அவற்றை சரியான அளவுகளுக்கு ஏற்ப கலந்து குளிர்விக்கத் தொடங்கவும்.
எனவே, தனித்துவமான பண்புகளைக் கொண்ட புதிய கலவையை உருவாக்க, பொருட்களின் அளவை சற்று மாற்றினால் போதும்.கூடுதலாக, புதிய அலாய் உற்பத்தி நிலைமைகளும் முக்கியமானவை: எடுத்துக்காட்டாக, உருகும் புள்ளி, துப்பாக்கி சூடு நிலைமைகள் அல்லது குளிரூட்டும் நேரத்தை மாற்ற இது போதுமானது.
அவற்றின் கலவையில் உலோகக் கலவைகளின் எதிர்ப்பின் சார்பு மிகவும் மாறுபட்ட தன்மையைக் கொண்டுள்ளது. சில சந்தர்ப்பங்களில், அலாய் என்பது கலவையை உருவாக்கும் இரண்டு உலோகங்களின் மிகச் சிறிய படிகங்களின் தொகுப்பாகும். ஒவ்வொரு உலோகமும் ஒருவருக்கொருவர் சுயாதீனமாக படிகமாக்குகிறது, அதன் பிறகு அவற்றின் படிகங்கள் ஒரே மாதிரியாகவும் தோராயமாகவும் கலவையில் கலக்கப்படுகின்றன.
இவை ஈயம், தகரம், துத்தநாகம் மற்றும் காட்மியம் ஆகியவை எந்த வகையிலும் கலக்கப்படுகின்றன. வெவ்வேறு செறிவுகளில் இத்தகைய உலோகக்கலவைகளின் எதிர்ப்பானது தூய உலோகங்களின் எதிர்ப்பின் தீவிர மதிப்புகளுக்கு இடையில் உள்ளது, அதாவது, அது எப்போதும் பெரியதை விட குறைவாகவும் சிறியதை விட அதிகமாகவும் இருக்கும்.
உலோக எதிர்ப்பு விவரங்கள்: கடத்தியின் எதிர்ப்பை எது தீர்மானிக்கிறது
மற்றொரு பயனுள்ள கட்டுரை: உலோகங்கள் மற்றும் உலோகக் கலவைகளின் அடிப்படை பண்புகள்
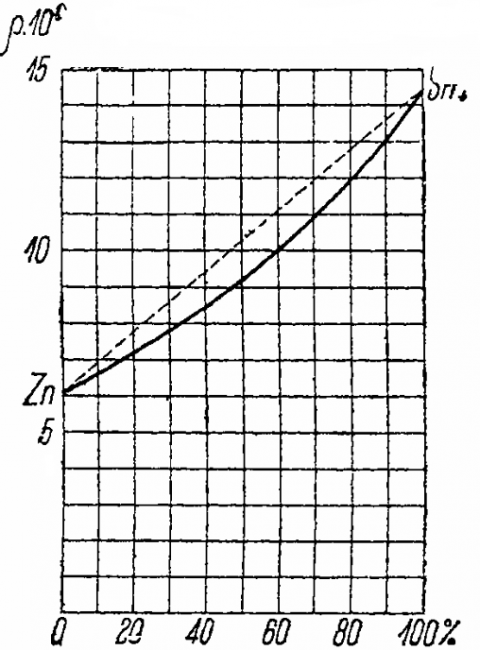
கீழே உள்ள படம் இரண்டு உலோகங்களின் தொகுதி செறிவு மீது ஒரு துத்தநாக-தகரம் கலவையின் எதிர்ப்பின் சார்புநிலையை வரைபடமாகக் காட்டுகிறது.
abscissa அலாய் யூனிட் அளவின் சதவீதமாக தகரத்தின் அளவைக் காட்டுகிறது, அதாவது. abscissa 60 என்பது அலாய் ஒரு யூனிட் அளவு 0.6 வால்யூம் டின் மற்றும் 0.4 அளவு துத்தநாகத்தைக் கொண்டுள்ளது. ஆர்டினேட் அலாய் ரெசிஸ்டிவிட்டி மதிப்புகளை 106 ஆல் பெருக்குவதைக் காட்டுகிறது.
தூய உலோகங்கள் என்பதால் எதிர்ப்பின் வெப்பநிலை குணகங்கள் வாயுக்களின் விரிவாக்கக் குணகத்திற்கு நெருக்கமான அதே வரிசையின் அளவுகள், கருதப்படும் குழுவின் உலோகக் கலவைகள் அதே வரிசையின் குணகங்களைக் கொண்டிருப்பது வெளிப்படையானது.
பல சந்தர்ப்பங்களில், இரண்டு உலோகங்களின் கலவைகள் இரண்டு உலோகங்களின் அணுக்களால் ஆன சிறிய படிகங்களால் ஆன ஒரே மாதிரியான வெகுஜனமாகும்.
சில நேரங்களில் இத்தகைய கலப்பு படிகங்கள் எந்த விகிதத்திலும் இரண்டு உலோகங்களின் அணுக்களிலிருந்து உருவாகலாம், சில சமயங்களில் இத்தகைய வடிவங்கள் செறிவூட்டப்பட்ட சில பகுதிகளில் மட்டுமே சாத்தியமாகும்.
இந்த பகுதிகளுக்கு வெளியே உலோகக்கலவைகள் இப்போது கருதப்பட்ட முதல் குழுவை ஒத்தவை, அவை தூய உலோகத்தின் படிகங்கள் மற்றும் இரண்டு வகையான அணுக்களால் ஆன கலப்பு வகை படிகங்களின் கலவையாகும்.
இந்த வகை உலோகக் கலவைகளின் எதிர்ப்பானது பொதுவாக இரண்டு உலோகங்களின் எதிர்ப்பை விட அதிகமாக இருக்கும்.

கீழே உள்ள படம், ஒவ்வொரு செறிவிலும் கலந்த படிகங்களை உருவாக்கும் தங்கம் மற்றும் வெள்ளி கலவையின் எதிர்ப்பின் செறிவு சார்ந்து இருப்பதை வரைபடமாகக் காட்டுகிறது. வளைவை உருவாக்கும் முறை முந்தைய படத்தில் உள்ள வளைவைப் போலவே உள்ளது.
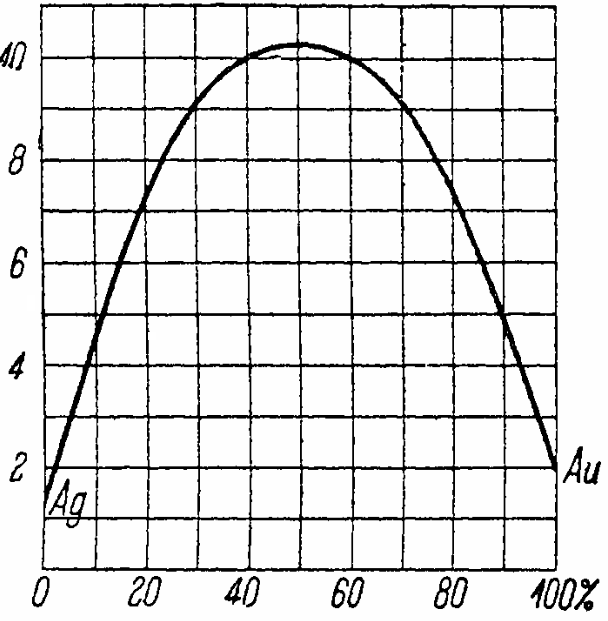
வரைபடத்தில் தூய வெள்ளியின் எதிர்ப்பானது 1.5 * 10-6, தூய தங்கம் 2.0 * 10-8... இரண்டு உலோகங்களின் சம அளவுகளை (50%) கலப்பதன் மூலம், 10.4 * 10- எதிர்ப்பைக் கொண்ட கலவையைப் பெறுகிறோம். 6.
இந்த குழுவின் உலோகக்கலவைகளுக்கான எதிர்ப்பின் வெப்பநிலை குணகங்கள் பொதுவாக கலவையை உருவாக்கும் ஒவ்வொரு உலோகத்தையும் விட குறைவாக இருக்கும்.
தங்கம் மற்றும் வெள்ளி கலவையின் வெப்பநிலை குணகம் தங்கத்தின் செறிவை சார்ந்திருப்பதை கீழே உள்ள படம் வரைபடமாக காட்டுகிறது.
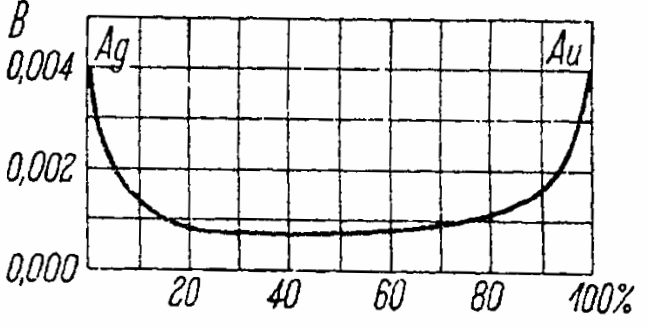
15% முதல் 75% வரையிலான செறிவுகளின் வரம்பில், எதிர்ப்பின் வெப்பநிலை குணகம் தூய உலோகங்களின் அதே குணகத்தின் கால் பகுதிக்கு மேல் இல்லை.
மூன்று உலோகங்களின் சில உலோகக்கலவைகள் தொழில்நுட்ப முக்கியத்துவம் வாய்ந்தவை.
இந்த உலோகக் கலவைகளில் முதன்மையானது, மாங்கனின், சரியாக செயலாக்கப்படும் போது, பூஜ்ஜியத்தின் வெப்பநிலை குணகம் உள்ளது, இதன் விளைவாக துல்லியமான எதிர்ப்பு இதழ்களை உருவாக்க மாங்கனின் கம்பி பயன்படுத்தப்படுகிறது.
நிக்கல், குரோமியம், மாங்கனீசு, சிலிக்கான், இரும்பு, அலுமினியம் (நிக்ரோம்) ஆகியவற்றின் கலவையானது பல்வேறு வெப்பமூட்டும் கூறுகளின் உற்பத்திக்கு மிகவும் பொதுவான பொருளாகும்.
இந்த வகை உலோகக் கலவைகள் பற்றிய கூடுதல் விவரங்கள்: நிக்ரோம்கள்: வகைகள், கலவை, பண்புகள் மற்றும் பண்புகள்
மீதமுள்ள உலோகக்கலவைகள் (கான்ஸ்டான்டன், நிக்கலின், நிக்கல் சில்வர்) ரியோஸ்டாட்களை ஒழுங்குபடுத்தும் உற்பத்திக்காகப் பயன்படுத்தப்படுகின்றன, ஏனெனில் அவை கணிசமான எதிர்ப்பைக் கொண்டுள்ளன, மேலும் ரியோஸ்டாட் கம்பிகள் அடிக்கடி கொண்டிருக்கும் அதிக வெப்பநிலையில் காற்றில் ஒப்பீட்டளவில் சிறிய ஆக்ஸிஜனேற்றம் கொண்டவை.
மின்சாரத் துறையில் பொதுவாகப் பயன்படுத்தப்படும் மும்மடங்கு கலவைகள் பற்றிய கூடுதல் விவரங்களுக்கு, இங்கே பார்க்கவும்:உயர் எதிர்ப்பு பொருட்கள், உயர் எதிர்ப்பு உலோகக்கலவைகள்
பல்வேறு உலோகக்கலவைகளின் குறிப்பிட்ட எதிர்ப்பு மதிப்புகளை சிறப்பு குறிப்பு புத்தகங்களில் பார்ப்பது அல்லது சோதனை ரீதியாக தீர்மானிப்பது சிறந்தது, ஏனெனில் அவை பரவலாக மாறுபடும்.
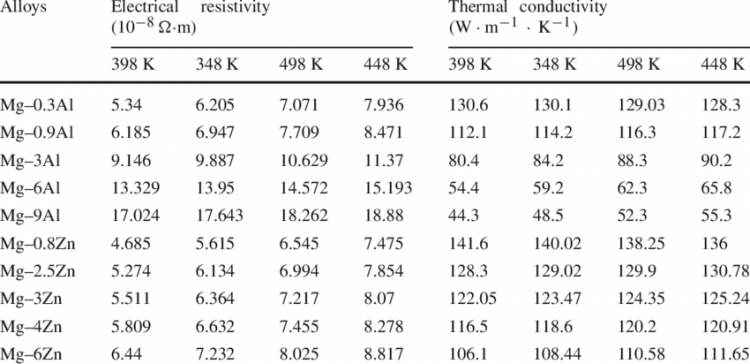
உதாரணமாக, Mg-Al மற்றும் Mg-Zn உலோகக் கலவைகளின் மின் எதிர்ப்பு மற்றும் வெப்ப கடத்துத்திறன் ஆகியவற்றின் மதிப்புகளை நாங்கள் தருகிறோம்:
இந்த வேலையில், Mg — Al மற்றும் Mg — Zn பைனரி உலோகக் கலவைகளின் மின் எதிர்ப்பு மற்றும் வெப்ப கடத்துத்திறன் 298 K முதல் 448 K வரையிலான வெப்பநிலை வரம்பில் ஆராயப்பட்டு, அதனுடன் தொடர்புடைய மின் கடத்துத்திறன் மற்றும் உலோகக் கலவைகளின் வெப்ப கடத்துத்திறன் ஆகியவற்றுக்கு இடையேயான தொடர்பு பகுப்பாய்வு செய்யப்படுகிறது.
மேலும் பார்க்க: மின் நிறுவல்களில் மிகவும் பொதுவான கடத்தும் பொருட்கள்